*Este post será atualizado periodicamente conforme novas informações sobre as vacinas surgirem.
Quais vacinas já foram aprovadas pela Anvisa?
Três vacinas já foram aprovadas pela Anvisa no Brasil.
Duas delas têm autorização apenas para uso emergencial: a Coronavac, produzida pelo laboratório chinês Sinovac em parceria com o Instituto Butantan, e a vacina de Oxford, produzida pelo laboratório Astrazeneca em parceria com a Universidade de Oxford, que foram aprovadas em 17 de janeiro. Esse registro permite apenas que elas sejam aplicadas em grupos prioritários e pelo sistema público de saúde. Nesse caso, a vacina ainda está em fase experimental e serve para atender à urgência imposta pela pandemia. Segundo Gustavo Mendes, responsável pela Gerência Geral de Medicamentos e Produtos Biológicos da Anvisa, alguns dados podem não estar totalmente consolidados e devem permanecer sob análise durante a imunização.
Já o imunizante da Pfizer, desenvolvido pelo laboratório americano em parceria com o alemão BioNTech, recebeu o registro definitivo em 22 de fevereiro. Isso significa que a farmacêutica tem permissão para comercializar doses para a iniciativa privada, além de poder fornecê-las ao SUS, e aplicá-las em toda a população acima de 16 anos. A vacina recebeu esse registro, porque apresentou dados consolidados e completos dentro do que a Anvisa chama de “padrão ouro”.
A vacina russa Sputnik V foi a única até agora que teve o pedido de uso emergencial rejeitado, pois o laboratório não entregou toda a documentação necessária.
Já o laboratório indiano Bharat Biotech, responsável pela produção da Covaxin, submeteu documentos apenas para aprovação das boas práticas de fabricação — que é uma fase anterior ao pedido de aprovação emergencial ou de registro definitivo.
Não há pedidos de outros laboratórios pendentes de avaliação pela Anvisa.
A vacina norte-americana da Moderna, produzida em parceria com os Institutos Nacionais da Saúde dos EUA, já foi aprovada emergencialmente no país e na União Européia.
A aprovação de qualquer vacina passa obrigatoriamente por três fases. A fase 1 testa a segurança em pequenos grupos de voluntários sadios, detectando e quantificando efeitos colaterais. Na fase 2, o teste ocorre em doses diferentes e em número maior de pessoas – algumas centenas. Na fase 3, ocorre o estudo de eficácia. Dessa vez, a vacina é aplicada em milhares de participantes – normalmente entre 1,5 mil e 5 mil pessoas –, e entre populações distintas, de diferentes regiões geográficas e nacionalidades.
A maioria dos laboratórios mediu apenas a prevenção contra o desenvolvimento da covid-19 e não contra a infecção pelo coronavírus. Significa que não é possível saber ainda se o medicamento vai impedir o contato com o vírus e a transmissão ou se vai apenas impedir o desenvolvimento da doença. A prova real da eficiência dessas medicações contra o coronavírus só será tirada mesmo quando a vacinação começar. Das vacinas compradas pelo governo brasileiro, apenas a Astrazena/Oxford divulgou a eficácia de 67% na redução da taxa de transmissão. A Coronavac, por exemplo, não tem esses dados demonstrados.
Segundo a imunologista Cristina Bonorino, professora da Universidade Federal de Ciências da Saúde de Porto Alegre e membro do Comitê Científico da Sociedade Brasileira de Imunologia, os cientistas só poderão afirmar a real eficácia das vacinas quando os dados forem submetidos para análise de especialistas e publicação em revistas científicas e a população começar a ser vacinada de fato.
Todos os brasileiros serão vacinados?
Embora fale em vacinar “todos os brasileiros”, o governo ainda não confirmou quando as pessoas que estão fora dos grupos de risco receberão a imunização. Segundo o Ministério da Saúde, o plano apresentado pelo governo não é definitivo e depende da aquisição de novas vacinas.
O governo federal prometeu em dezembro 300 milhões de doses — 260 milhões de doses e insumos para fabricação da vacina da Astrazeneca/Oxford pela Fiocruz com custo estimado de R$ 1,9 bilhão, e 42,5 milhões de doses do consórcio Covax Facility, que ainda não tem nenhuma vacina aprovada.
A Fiocruz nos disse que já foram entregues 4 milhões de doses ao Ministério da Saúde e há outras oito milhões importadas que estão para chegar nos próximos meses. O segundo contrato feito entre o governo federal e o laboratório corresponde à encomenda tecnológica para produção nacional da vacina de Oxford. A previsão é de que sejam produzidas 100,4 milhões de doses até julho e mais 110 milhões até dezembro, somando um total de 210,4 milhões.
O governo também anunciou em dezembro que havia a possibilidade de comprar mais 70 milhões de doses da norte-americana Pfizer. Embora ela já tenha sido aprovada pela Anvisa, não há informação de compra de doses até o momento. O problema dessa vacina é que ela precisa ser armazenada a 70ºC abaixo de zero, e não há equipamentos que suportem essa temperatura no SUS. Uma das possibilidades é de que a vacina seja armazenada em gelo seco por 15 dias. Ela também pode ser mantida entre 2°C e 8°C por no máximo cinco dias.
No dia 25 de fevereiro, o Ministério da Saúde divulgou que a pasta assinou um contrato no valor de R$ 1,6 bilhão para comprar 20 milhões de doses da indiana Covaxin junto à Precisa Medicamentos/Bharat Biotech. Essa vacina, no entanto, ainda não foi aprovada pela Anvisa.
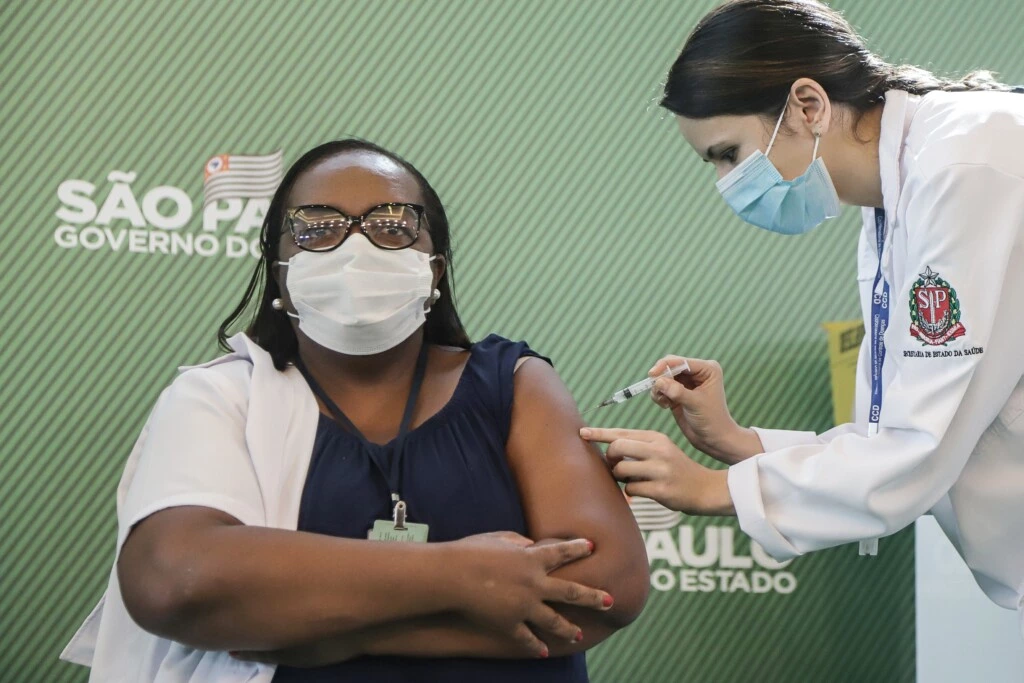
Foto: Foto: Rahel Patrasso/Xinhua via Getty Images
Quando serei vacinado?
A primeira pessoa a ser imunizada no Brasil foi a enfermeira Monica Calazans, 54, que trabalha na UTI do Instituto de Infectologia Emílio Ribas, em São Paulo. Ela foi vacinada com a CoronaVac no dia 17 de janeiro, logo após a aprovação do uso emergencial da vacina pela Anvisa.
Até o dia 24 de fevereiro, 6.087.811 haviam recebido a primeira dose de uma das vacinas disponíveis pelo SUS, o que equivale a 2,87% da população brasileira. As aplicações representam 52,07% das doses recebidas pelos estados. Os dados são atualizados diariamente por um consórcio de veículos de imprensa, com base em informações repassadas pelos estados, uma vez que o governo federal não disponibiliza o mapeamento da vacinação no país.
O Plano Nacional de Imunização do Ministério da Saúde, o PNI, prevê a compra de 350 milhões de doses de vacinas contra a covid-19 para 2021, suficientes para vacinar 175 milhões de pessoas, já que cada pessoa precisa tomar duas doses. Até 24 de fevereiro, no entanto, haviam sido adquiridas 11 milhões de doses da CoronaVac e quatro milhões da vacina da Oxford (lotes já entregues). Há previsão de aquisição de um total de 100 milhões de doses do Butantan até agosto e 110,4 milhões de doses da Oxford até dezembro.
Após uma atualização publicada em nota técnica, o PNI está considerando como grupo prioritário da primeira fase os trabalhadores que atuam na linha de frente da saúde, a população idosa residente em instituições de longa permanência, pessoas a partir de 18 anos com deficiência que vivem em residências inclusivas, povos indígenas que vivem em terras homologadas e idosos da região norte do país, cujo cálculo leva em consideração grupos de idosos que vivem nos estados Rondônia, Amapá, Tocantins e Amazonas. Nós solicitamos esclarecimentos sobre essa atualização no dia 25 de fevereiro, mas até agora não recebemos resposta do Ministério de Saúde.
Como a quantidade de vacinas adquiridas até agora é insuficiente para vacinar todas as pessoas do primeiro grupo risco, os estados estão dando prioridade aos mais vulneráveis dentro do grupo, como os idosos acima de 80 anos, por exemplo.
Na segunda etapa, entram pessoas de 60 a 74 anos. Na terceira, serão imunizadas as pessoas com comorbidades que apresentam maior chance para agravamento da doença como portadores de doenças renais crônicas e cardiovasculares.
A quarta fase, que previa a vacinação de professores e forças de segurança, foi excluída em janeiro. Crianças, gestantes e os demais grupos não foram citados pelo plano nacional.
As comorbidades consideradas pelo Ministério da Saúde são: diabetes mellitus, hipertensão, doença pulmonar obstrutiva crônica, doença renal, cardiovasculares e cerebrovasculares; indivíduos transplantados de órgão sólido, anemia falciforme, câncer e obesidade grave (IMC>/40).
Não há informações sobre quando pessoas fora do grupo de risco e que não trabalham em áreas essenciais serão vacinadas. Ou seja, se você tem entre 18 e 59 anos, nenhuma comorbidade e não trabalha nas áreas de saúde, educação e segurança, pode-se considerar no fim da fila.
Uma complicação que atrasou o processo foi a compra de agulhas e seringas, que o governo demorou a licitar. No fim de dezembro, o Ministério da Saúde abriu um pregão para comprar 331 milhões de seringas, mas só conseguiu oferta para 7,9 milhões – 2,4% do total de unidades que a pasta desejava adquirir. Após o fracasso na compra, o governo restringiu a exportação de seringas e agulhas alegando que o material é necessário para a vacinação em massa contra a covid-19 e requisitou 60 milhões de seringas às indústrias do setor.
Quais vacinas foram compradas pelo governo federal?
O Ministério da Saúde já adquiriu 11 milhões de doses da Coronavac, produzida pelo laboratório chinês Sinovac em parceria com o Instituto Butantan. O contrato prevê a compra de 46 milhões de doses até abril, mais 54 até agosto. O Ministério solicitou recentemente mais 30 milhões de doses além dessas 100 milhões, mas o instituto não quer manter o contrato de exclusividade com o governo federal, pois há solicitações de estados e municípios na fila.
Outro acordo formalizado pelo Ministério da Saúde foi com a Fiocruz, para aquisição de 100,4 milhões de doses da vacina da Astrazeneca/Oxford até julho, mais 110 milhões de doses entre agosto e dezembro. A negociação também inclui a transferência total da tecnologia para que as vacinas sejam produzidas aqui pela Fiocruz.
Até 25 de fevereiro, o governo havia importado quatro milhões de doses da vacina da Astrazeneca/Oxford produzidas pelo laboratório indiano Serum, em parceria com a empresa indiana de biotecnologia Bharat Biotech, para antecipar a vacinação. Outras oito milhões de doses devem chegar nos próximos meses.
Também há um acordo para a compra de 42,5 milhões de doses da Covax Facility, aliança mundial de vacinas contra a covid-19 capitaneada pela Organização Mundial de Saúde. No dia 9 de fevereiro, a Anvisa aprovou uma resolução que dispensa registro e autorização emergencial das vacinas compradas por meio do consórcio, que inclui 150 países e foi criado pela Organização Mundial da Saúde para facilitar o acesso aos imunizantes. Há especialistas da Anvisa entre os responsáveis pela análise dos estudos das vacinas produzidas pelo consórcio.
No dia 10 de dezembro, o governo federal assinou um protocolo de intenção de compra para adquirir mais 70 milhões de doses da norte-americana Pfizer e 38 milhões de doses da vacina da francesa Janssen.
Quais estados estão negociando vacinas?
Com a imunização a passos lentos pela inação do governo federal, estados e municípios se articulam para adquirir doses e comandar a própria campanha de vacinação. Mas os contratos firmados até agora pelos laboratórios dos imunizantes aprovados pela Anvisa foram exclusivamente com o governo federal, formando uma fila única de vacinação. O Instituto Butantan, que produz a Coronavac, firmou dois contratos com o Ministério da Saúde com cláusula de exclusividade. Por enquanto, cabe ao Programa Nacional de Imunização do Ministério distribuir essas doses aos estados.
São Paulo é o primeiro estado na fila de solicitações ao Butantan. O governo estadual manifestou interesse em comprar 20 milhões de vacinas extras para imunizar sua população. A demanda, segundo o instituto, só poderá ser atendida após a entrega das 100 milhões de doses contratadas pelo Ministério da Saúde, cuja conclusão está prevista para agosto.
A promessa de João Doria é vacinar 9 milhões de pessoas na primeira fase, o equivalente a 18 milhões de doses, já que são necessárias duas aplicações do imunizante. São Paulo também havia anunciado que pretende disponibilizar mais 4 milhões de doses produzidas em parceria com o Instituto Butantan para outros estados. Pelo menos 11 estados e 276 municípios formalizaram interesse na aquisição do imunizante. Os estados interessados são: Acre, Pará, Maranhão, Roraima, Piauí, Mato Grosso do Sul, Espírito Santo, Rio Grande do Norte, Paraíba, Ceará e Rio Grande do Sul.
A vacina será vendida na rede privada?
O Ministério da Saúde nos disse que os laboratórios produtores de vacinas têm autonomia para comercializar as vacinas com a rede privada, desde que as vacinas compradas tenham sido regulamentadas pela Anvisa. A agência reguladora, por sua vez, confirmou que qualquer vacina aprovada pela agência estará disponível tanto para a rede pública quanto para a privada. Os gestores estaduais também têm autonomia para fazerem aquisições das vacinas. A Associação Brasileira das Clínicas de Vacinas informou neste domingo, 3, que está negociando a compra de 5 milhões de doses da Covaxin.
Como está sendo a logística de vacinação?
Em dezembro, quando a vacinação já havia começado no exterior, o Ministério da Saúde ainda não sabia informar detalhes de como seria realizada a vacinação da população no Brasil. Por e-mail, nos respondeu que estava preparado em função da rede já existente de imunização para outras doenças. Quase dois meses depois, em 25 de fevereiro, entretanto, o ministério diz que distribuiu apenas cerca de 15 milhões de doses. Até o dia 28 de fevereiro, o mapa da vacinação no Brasil — monitoramento feito por consórcio de veículos de imprensa a partir de dados das secretarias estaduais — indicava que pouco mais de 6,5 milhões de brasileiros haviam recebido ao menos uma dose do imunizante, o que corresponde a apenas 3,11% da população nacional.
A vacina vai resolver a pandemia?
Ainda não. Para que a vacinação em massa tenha o efeito desejado de reduzir a circulação do vírus, especialistas afirmam que é preciso manter o afastamento social até que boa parte da população mundial seja vacinada. Segundo o presidente do Comitê Científico da Sociedade Brasileira de Imunologia, João Viola, é preciso vacinar de 40% a 50% da população para alcançar a chamada “imunidade de rebanho”, que ele prefere definir como “imunidade comunitária”.
Se todos os países começassem a vacinar em janeiro, por exemplo, e a vacinação transcorrer sem problemas, seria possível alcançar esse cenário no segundo semestre de 2021. O mesmo cálculo pode ser feito proporcionalmente à população de cada país, mantendo os protocolos já conhecidos de isolamento e outras medidas de prevenção como uso de máscaras.
Mas o governo federal não tem ajudado. Deixando a saúde pública de lado, o general Eduardo Pazuello afirmou no dia 2 de dezembro que não se pode mais falar em afastamento social já que, na avaliação dele, a campanha para as eleições municipais ocorreu com aglomeração e não houve aumento de contaminação. “Se esse vírus se propaga por aglomeração, por contato pessoal, por aerossóis e nós tivemos a maior campanha democrática que podia ter no nosso país, que é a municipal, nos últimos dois meses, se isso não trouxe nenhum tipo de incremento ou aumento em contaminação, não podemos falar mais em lockdown nem nada”, disse o ministro. Isso depois de o presidente Jair Bolsonaro ter desacreditado a vacinação em diversas ocasiões.
Em janeiro, o Supremo Tribunal Federal atendeu ao pedido do procurador-geral da República Augusto Aras e abriu um inquérito para investigar a conduta do ministro em relação à falta de oxigênio nos hospitais de Manaus.
Também não há segurança de que as vacinas terão a taxa de eficácia prometida. Para Cristina Bonorino, imunologista e membro do Comitê Científico da Sociedade Brasileira de Imunologia, esse resultado só será posto à prova quando a população for vacinada. “Meu feeling pessoal é de que deveria se esperar um pouco mais sem acelerar os estudos. Por outro lado, que bom que parecem estar funcionando bem. Não dá para acreditar e nem desacreditar 100%”, afirma.
Os especialistas também se preocupam com as recentes aglomerações, especialmente durante o Carnaval, que acabam facilitando a circulação do vírus e o surgimento de possíveis novas variantes.
O que é a vacina e como ela funciona?
As vacinas são desenvolvidas a partir da observação das reações do próprio organismo em contato com vírus ou qualquer outro microorganismo. Quando há uma infecção, o corpo faz uma resposta imunológica contra os agentes da doença e, na grande maioria das vezes, desenvolve uma resposta imune protetora, como acontece com a catapora e o sarampo.
Para desenvolver uma vacina, explica o pesquisador Viola, componentes dos agentes infecciosos são modificados para não causar mais doenças. Esses microorganismos que não causam mais infecção são usados na vacina para fazer a resposta protetora.
A vacina mais rápida já desenvolvida antes do coronavírus foi a da caxumba, que levou quatro anos. Mas normalmente esse prazo é bem maior, entre 10 a 15 anos. A vacina da varíola, por exemplo, levou quase 20 anos para ficar pronta. E há casos como o da dengue, que é uma doença conhecida há quase 20 anos e ainda não se descobriu a vacina e até mesmo a malária, que mesmo tendo uma vacina contra a doença sendo estudada há mais de 30 anos nunca teve um resultado eficaz.
Qual a proteção das vacinas disponíveis?
Segundo a imunologista Bonorino, existem três tipos de proteção induzíveis por uma vacina: a proteção contra infecção, que evita a transmissão do vírus (feita por anticorpos neutralizantes, que bloqueiam a entrada do vírus na célula); a proteção da doença com sintomas leves e a proteção da doença com sintomas graves. Nenhum dos estudos de vacina testou a eficácia contra a infecção da doença e a consequente transmissão do coronavírus. O que se testou foi a inibição do desenvolvimento da covid-19. Quer dizer que você pode entrar em contato com o vírus, mas não vai ficar doente. Para testar a infecção seria necessário testar semanalmente voluntários para material genético do vírus, pelo exame de PCR (aquele do cotonete no nariz). Além de caro, esse processo levaria mais tempo para ser finalizado.
Até agora, as vacinas têm mostrado proteção contra o desenvolvimento da doença. Ou seja, a vacina vai barrar o vírus antes que ele consiga provocar algum sintoma. Mas é possível que o indivíduo imunizado ainda possa contrair o vírus e passá-lo adiante, mesmo que não apresente sintomas.
Natália Pasternak, microbiologista e presidente do Instituto Questão de Ciência, acrescenta que testes feitos em animais indicaram que alguns deles ainda tinham resquícios do vírus no nariz após a vacinação, mas ninguém mediu se esse vírus ainda estava ativo. “Por isso, é preciso continuar com as medidas de prevenção mesmo após ser vacinado até que a maior parte da população seja vacinada e a gente consiga, realmente, adquirir imunidade de rebanho”, alertou.
Foto: Andre Coelho/Getty Images
Quanto tempo dura a imunidade da vacina?
Por enquanto, não é possível saber por quanto tempo vai durar a imunidade proporcionada pela vacina. O pesquisador Viola acredita que a comunidade científica só terá uma projeção daqui um ou dois anos e que novos estudos serão necessários.
As vacinas em teste contra o coronavírus têm efeitos colaterais?
Os efeitos colaterais provocados pelas vacinas como um todo são raros e brandos. Com as vacinas testadas até agora contra o coronavírus não é diferente. Poucas pessoas apresentaram febre e mal estar leve e passageiro. É possível que haja uma pequena reação no local da aplicação da vacina, mas nada que seja preocupante. Há relatos, assim como em casos da vacina contra a gripe, de resfriado leve de um a dois dias. Nenhum efeito colateral mais grave foi relatado até agora.
Quais vacinas foram testadas no Brasil?
Temos quatro vacinas sendo testadas no Brasil: a Astrazeneca/Oxford, a Coronavac, a Pfizer-BioNtech e uma vacina desenvolvida pela farmacêutica Janssen-Cilag da Johnson & Johnson que ainda não teve a eficácia divulgada. Somos um bom laboratório para esse tipo de testes devido à diversidade da população brasileira e aos altos índices de infecção pelo coronavírus que já levou à morte de mais de 170 mil pessoas.
Qual a eficácia de cada uma das vacinas?
Um estudo publicado recentemente na revista The Lancet, uma das mais renomadas publicações científicas do mundo, atualizou a eficácia da vacina desenvolvida pela Astrazeneca/Oxford. No ano passado, o laboratório havia apresentado dados diferentes, dependendo da dose que os pacientes tomaram, o que provocou questionamentos por parte da comunidade científica. Por isso, algumas pesquisas precisaram ser refeitas, o que também atrasou a sua aprovação.
A vacina está sendo testada no Brasil por meio da Fiocruz, que passará a produzi-la, o que permite acompanhamento da pesquisa pela Anvisa. O último estudo publicado mostrou que a vacina tem eficácia de 76% entre o 22º dia e o 90º dia após a aplicação da primeira dose. Após a segunda dose, a eficácia é de 82,4%, considerando um período de 20 dias. Além disso, a vacina de Oxford reduz em 67% a transmissão da doença. Essas porcentagens divulgadas são referentes aos sintomas leves, para sintomas graves a eficácia é maior.
É importante deixar claro que a porcentagem de eficácia que está sendo divulgada pelos laboratórios representa o potencial de pessoas protegidas com determinada vacina. Se a eficácia de uma vacina é de 94%, por exemplo, significa que 94% das pessoas que tomaram a vacina ficaram protegidas contra a doença.
A vacina da Moderna-Institutos Nacionais da Saúde dos EUA teve eficácia de 94,5% depois de ser testada em cerca de 30 mil pessoas. O valor estimado por dose é de 21 euros, contra 3 euros a dose da Astrazeneca/Oxford. Primeira a ser aprovada por uma agência reguladora, a vacina da Pfizer-BioNtech teve eficácia divulgada parecida, de 95%. O valor estimado dessa vacina é de 15 euros por dose. Já a russa Sputnik V do Instituto Gamaleya, teve, o governo da Rússia, eficácia de 91,4%. O valor estimado é de até 10 dólares por dose.
Após anunciar que a CoronaVac teve 100% de eficácia para casos graves e moderados de covid-19 e 78% para os infectados que apresentaram casos leves ou precisaram de atendimento ambulatorial, o Butantan divulgou no dia 12 a eficácia global da CoronaVac. Os dados mostram uma taxa de 50,38%.
Apesar de a taxa de eficácia da Coronavac superar por pouco o limite de 50% estipulado pela OMS para aprovar as vacinas contra a covid-19, ela é semelhante a de vacinas já em uso, como a de rotavírus e coqueluche, e acima da vacina contra a gripe. A vacina apresentou eficácia de 78% na prevenção de sintomas leves e 100% na prevenção de sintomas graves.
Qual a temperatura de armazenamento das vacinas?
Além de toda a logística de produção e distribuição das vacinas, outra questão que os governos têm enfrentando é o armazenamento.
As principais vacinas cogitadas pelo governo federal e de São Paulo são as que atendem à capacidade de armazenamento disponível na rede pública brasileira e têm um custo de produção menor. A Astrazeneca/Oxford, por exemplo, pode ficar armazenada em temperatura entre 2º e 9º graus, mesma temperatura das outras vacinas armazenadas pelo SUS. A Coronavac também pode ser conservada entre 2º e 8º C.
Já a vacina desenvolvida pela Moderna até pode ser conservada em temperaturas entre 2º e 8º graus, mas nesse caso, só teria durabilidade de 30 dias. Agora, se for conservada 20º graus abaixo de zero, pode durar por até seis meses, mas dependeria de uma estrutura que o SUS não dispõe. A russa Sputnik V também precisa de capacidade de armazenamento a 18º graus negativos.
Quais as fontes deste texto e onde acho mais informações confiáveis?
Mapa das vacinas em teste no Brasil (Anvisa)
Exposição Covid-19 (Sociedade Brasileira de Imunologia)
Vacinas Covid-19 (Organização Mundial de Saúde, em inglês)
Dados e números diários da Covid-19 no Brasil (Ministério da Saúde)
Vacinas contra a Covid-19 (Fiocruz)
Our World in Data (Dados sobre quantas pessoas já foram vacinadas e em que países organizado pela Universidade de Oxford, em inglês)
Temos uma oportunidade, e ela pode ser a última:
Colocar Bolsonaro e seus comparsas das Forças Armadas atrás das grades.
Ninguém foi punido pela ditadura militar, e isso abriu caminho para uma nova tentativa de golpe em 2023. Agora que os responsáveis por essa trama são réus no STF — pela primeira e única vez — temos a chance de quebrar esse ciclo de impunidade!
Estamos fazendo nossa parte para mudar a história, investigando e expondo essa organização criminosa — e seu apoio é essencial durante o julgamento!
Precisamos de 800 novos doadores mensais até o final de abril para seguir produzindo reportagens decisivas para impedir o domínio da máquina bilionária da extrema direita. É a sua chance de mudar a história!
Torne-se um doador do Intercept Brasil e garanta que Bolsonaro e sua gangue golpista não tenham outra chance de atacar nossos direitos.